Skriv ut
Utredning ved kreft i tykk- og endetarm
Prioritering
Ved mistanke om tarmkreft må pasienten uten opphold utredes for å stille sikker diagnose. Dersom kreft blir påvist må sykdommens utbredelse kartlegges umiddelbart. Dette gir grunnlag for optimal behandling.
Helsedirektoratet har laget en veiledning når det gjelder prioritet for utredning. De definerer følgende alarmsymptomer: Vekttap, endret avføringsmønster, blod i avføring. Hvis minst ett av disse alarmsymptomer oppstår, er veiledende frist for helsehjelp 3 uker. Veilederen sier videre at dersom det oppstår frisk rektalblødning hos pasient over 45 år og det er begrunnet mistanke om kreft i mage-tarm-kanalen, så er veiledende frist for start av helsehjelp 2 uker.
I ordningen for pakkeforløp ved kreft anføres at det er begrunnet mistanke om kreft i tykk- og endetarm hos pasienter over 40 år med ett eller flere av følgende symptomer eller funn:
- Uavklart blødning fra tarmen
- Funn av svulst eller polypp ved rektoskopi
- Endring av et ellers stabilt avføringsmønster som varer i mer enn fire uker
| Hvis symptomene ovenfor foreligger skal fastlegen henvise til pakkeforløp, og dette skal registreres ved mottakende sykehus og gir følgende rettigheter: |
| Fra henvisning mottatt til første fremmøte for utredning |
Maks 9 kalenderdager |
| Fra første fremmøte til avsluttet utredning |
Maks 12 kalenderdager |
| Fra avsluttet utredning til start behandling (kirurgi) |
Maks 14 kalenderdager |
Klinisk undersøkelse
Det foretas intervju av pasienten for å kartlegge nyoppståtte symptomer samt tidligere gjennomgått og eventuelt pågående sykdom og medikamentbruk. Alle disse forhold kan påvirke valg av behandling.
Det gjøres full klinisk undersøkelse og det viktigste er da å undersøke magen, dessuten gjøre en undersøkelse av endetarmen med finger (rektal eksplorasjon). Man sjekker om det er synlig blod på hansken. Dersom så ikke er tilfelle, tester man på usynlig blod ved å dryppe test-væske på avføringen.
Blodprøver
Det tas blodprøver med minimum blodprosent, samt nyre- og leverprøver, og man måler nivået av et et protein kalt carcinoembryonalt antigen (CEA) i blodet. Den viser forhøyet verdi hos om lag halvparten av pasientene. Dersom den er betydelig forhøyet, er det ofte en indikasjon på utbredt sykdom med dårlig prognose. Den viktigste bruken av CEA er å måle nivået rett etter operasjon for å se at den faller til normalverdi, deretter å følge den ved kontroller fordi ny stigning av CEA kan indikere tilbakefall av kreftsykdommen etter en antatt kurativ operasjon.
Skopi og vevsprøver
Innvendig undersøkelse av tarmen med en fiberoptisk slang kalles skopi eller endoskopi. Undersøkelse av venstre del av tykktarmen kalles sigmoideoskopi, av hele tykktarmen kalles koloskopi.
Nedre del av tarmen (endetarmen og litt av tykktarmen) opp til nivå 15-20 cm fra endetarmsåpningen kan også undersøkes med et stivt skop, dette kalles rektoskopi.
Skopi gir i de aller fleste situasjoner betydelig bedre og sikrere informasjon om polypper og svulster i tarmen enn det som oppnås med røntgenundersøkelser. Dessuten kan man via skopene ta vevsprøver og man kan fjerne polypper dersom de ikke er for store.
Her kan du lese mer om ano-/rektoskopi >>>
Her kan du lese mer om koloskopi >>>
.png)
Koloskopi/CT-kolografi
Man tilstreber å gjøre full koloskopi før operasjonen, men når det er stenose i tarmen på grunn av stor svulst, er det ikke alltid passasje for skopet og man får ikke undersøkt tarmen ovenfor svulsten. Da kan man supplere med CT kolografi. Dagen før den undersøkelsen drikker man et kontrastmiddel som vil legge seg på slimhinnen. Ved undersøkelsen fyller man opp tarmen med CO2-gass via endetarmskanalen. Man får da framstilt alle områder av tarmen selv om det foreligger svulst med stenose for skop. Det kan også være lettere å vise svulstens presise lokalisasjon i tykktarmen ved kolografi enn ved koloskopi. CT kolografi er meget treffsikker når det gjelder å påvise kreftsvulster og polypper som er større en 1 cm, mens mindre polypper kan overses.
Dersom det ikke kunne gjøres komplett koloskopi før operasjonen, skal det gjøres ny koloskopi cirka 3 måneder etter operasjonen, og det er da vanligvis ikke noe problem å undersøke hele den gjenværende del av tarmen.
Både før koloskopi og CT kolografi må tarmen tømmes grundig dagen før undersøkelsen, og dette er en ganske slitsom prosedyre. Koloskopi tar 15–60 minutter og plagene ved undersøkelsen varierer fra nesten ingen smerter til betydelige smerter. Man får smertestillende og avslappende medisin for å redusere plagene. CT kolografi tar cirka 20 minutter og de fleste har lite smerter.
Koloskopi med fleksibelt skop er også den mest skånsomme metoden for å påvise svulst i endetarmen, selv om disse også kan ses ved rektoskopi. Når det er en kreftsvulst i endetarmen er det gjerne trangt og rektoskopi med det stive skopet er ofte smertefullt og det kan være vanskelig å se øvre deler av svulsten. Det er mindre smerter og man får bedre oversikt dersom man bruker et fleksibelt skop for å undersøke rektum.
Et fleksibelt skop kan ligge i betydelig bøy/sving når man undersøker endetarmen og nedre del av tykktarmen, og det er derfor vanskelig å måle eksakt hvor langt opp i tarmen svulsten ligger. Dersom nivået måles til mindre enn 25 cm opp fra endetarmsåpningen med fleksibelt skop, må det gjøres rektoskopi med stivt skop slik at man kan måle eksakt avstand fra endetarmsåpningen og til nedre kant av svulsten. Dette er viktig for å avklare om man må fjerne hele endetarmen og legge stomi som varig løsning, eller om man kan beholde en liten rest av endetarmen slik at det kan legges tarmskjøt (anastomose) mellom tykktarmen og endetarm-resten, slik at pasienten kan unngå permanent stomi.
Vevsprøver (biopsier)
Både ved kolo- og rektoskopi må det tas vevsprøver av mistenkt svulst. Disse prøvene tas med en liten tang som føres inn gjennom koloskopets arbeidskanal, eller større tenger som kan føres inn via rektoskop. Ofte består en svulst av områder der det er kreftutvikling og andre områder der det fortsatt er bare godartet polyppvev. Biopsiene må derfor tas fra områder som gir mest mistanke om kreftutvikling. Det er ikke alltid så enkelt å komme i posisjon med skopet slik at man får tatt prøve fra mest suspekte sted, og noen ganger kan det være vanskelig å få ut prøver fra kreftområdet fordi svulsten her er svært hard. Det er derfor ikke uvanlig at man ikke får tatt en representativ prøve med sikker bekreftelse på infiltrerende kreft. Dersom svulsten ut fra utseende utvilsomt er en kreftsvulst og biopsien viser minst høygradig dysplasi, er diagnosen kreft sikker. Dersom utseendet ikke er helt opplagt og man ser kun moderat dysplasi ved mikroskopisk undersøkelse, må det tas nye vevsprøver for avklaring.
Animasjonsvideo av rektal eksplorasjon og av nålebiopsi (vevsprøve) av lesjon utenfor tarmveggen
Bildediagnostikk for å kartlegge lokal og regional sykdomsutbredelse
Det er viktig å kartlegge hvor dypt svulsten vokser i tarmveggen og om den eventuelt vokser utenfor tarmveggen og eventuelt inn i naboorganer, og det er viktig å kartlegge eventuell spredning til lymfeknuter i tarmkrøset.
Bildeundersøkelser av endetarmen
Transrektal ultralyd
Ved tidlige svulster i endetarmen, det vil si svulster som vokser bare overflatisk i tarmveggen (mukosa / submukosa) er ultralyd best for å vurdere dybdevekst. Dersom svulsten vokser bare i øvre del av submukosa laget, kan det være aktuelt å gjøre lokal eksisjon (fjernelse) av svulsten og dermed unngå stor operasjon som eventuelt kan medføre total fjernelse av endetarmen og permanent stomi.
MR av endetarm/bekken
For alle svulster i rektum, unntatt de helt overflatisk voksende, er MR overlegen når det gjelder å bestemme hvor dypt ned i tarmveggen svulsten vokser, og å kartlegge om det foreligger spredning til lymfeknuter, og om det kan foreligge karinnvekst (svulsten vokser inn i blodårer utenfor tarmveggen).
Ved MR kan man også måle avstanden fra hovedsvulsten, lymfeknutene og fra eventuell karinnvekst og ut til fascien (bindevevshinnen) som omgir fettvevet utenfor tarmveggen, denne kalles for den mesorektale fascie. Dersom denne avstanden er kort (2 mm eller mindre) er det grunnlag for å gi forbehandling med bestråling og eventuell cellegift før operasjonen. Dette vil oftest føre til at svulsten skrumper noe, og det er da lettere å oppnå frie marginer rundt svulsten når den opereres ut, det vil si at man får gjort en kirurgisk radikal operasjon slik at det ikke er noe gjenværende svulstvev. Dette kalles R0-reseksjon (Residual tumor = 0). MR viser også forholdene på bekkenveggen, herunder om det er tegn til spredning til lymfeknutene her og man kan se større blodårer og nerver og svulstens relasjon til disse.
Bildeundersøkelser av tykktarmen
CT abdomen/CT kolografi
Ved moderne såkalt spiral CT med multislice-teknikk tas det flere «lag» med bilder og disse kan bygges opp til et tredimensjonalt bilde. Ved denne teknikken kan man få en god indikasjon på svulstens dybdvekst og relasjon til omgivelsene.
Ved CT kolografi (se ovenfor) blåser man inn gass i tarmlumen slik at tarmen åpnes og spiles ut, og man kan da få enda bedre bilder for å vurdere forholdene. Man får bedre oversikt om svulsten vokser utenfor tarmveggen og inn i nærliggende organer/strukturer, hvilket kan gi grunnlag for forbehandling før operasjonen, og dette kan også ha betydning for valg av operasjonsmetode.
Ved disse undersøkelsene kan man også se om det er forandringer av lymfeknutene i det regionale tarmkrøset og eksakt lokalisasjon av disse. En lymfeknute som er forstørret, har endret form med uregelmessig kontur av kapselen og inhomogent innhold (sentralt henfall ved nekrose), gir mistanke om at det foreligger kreftspredning til lymfeknuten.
CT med karmapping
Man kan sette kontrast i blodårene og gjøre detaljert undersøkelse av de anatomiske forhold til blodårene som fører blodet inn til tarmen (arterier) og årene som fører blodet bort fra tarmen igjen (vener). Det er betydelige anatomiske variasjoner av disse blodårene, og en kartlegging av blodårenes forløp før operasjonen kan være til hjelp for kirurgen under operasjonen, da det er viktig å frilegge og dele blodårene på korrekt sted.
Undersøkelse av fjernspredning
CT av mage (abdomen) og bekken
Dette gjøres alltid ved kreft i både tykktarm og endetarm og man leter da spesielt etter tegn til kreftspredning i leveren og i bukhulen, til lymfeknuter langs hovedpulsåren og inn mot leveren, dessuten også i binyre og eggstokker.
CT av lungene og brystskilleveggen (Ct-thorax og mediastinum)
Dette gjøres alltid og man kan da påvise eventuelle spredningssvulster i lunge og/eller til lymfeknuter i mediastinum.
MR av lever
Dersom CT gir mistanke om metastase(r) i leveren gjør man vanligvis supplerende MR av leveren med spesielt kontrastmiddel. Denne undersøkelsen er både mer sensitiv (oppdager flere lesjoner) og mer spesifikk enn CT (karakteriserer lesjonen bedre, det vil si skiller bedre mellom ondartede og godartede lesjoner).
PET-scan (PET-CT)
Ved denne undersøkelsen skannes hele kroppen etter at det er satt kontrast med radioaktivt stoff som binder seg til kreftceller, og det kan gi tilleggsinformasjon om fjernspredning. PET-Ct gjøres ikke rutinemessig, men kan være aktuelt dersom det er stor mistanke om fjernspredning (for eksempel meget høy CEA), mens CT/MR ikke har vist spredning.
Klassifisering av sykdomsutbredelse/stadium
Klinisk stadium
På bakgrunn av all informasjon man har før operasjonen, det vil si klinisk undersøkelse, endoskopi, vevsprøver og røntgen-undersøkelser defineres det kliniske sykdomsstadium, og i henhold til dette får man avklart om behandlingsintensjonen er kurativ (man kan potensielt fjerne alt kreftvev), potensielt kurativ eller palliativ (det er åpenbart ikke mulig å fjerne alt kreftvev og helbrede pasienten).
På bakgrunn av klinisk stadium bestemmer man det også om det er grunnlag for forbehandling før operasjon. Dette drøftes i et tverrfaglig team med kirurger, onkologer (kreftleger), radiologer og eventuelt patologer.
Histo-patologisk undersøkelse og klassifisering
Vevsprøver tatt før operasjonen blir undersøkt i mikroskop. Dersom pasienten blir operert blir operasjonspreparatet fiksert i formalin og etter noen dager gransket av patologer, både hvordan prepraratet ser ut med det blotte øyet (makroskopisk) og i mikroskopet. Granskningen innebærer flere elementer som gjennomgås nedenfor.
Hvilken kreft-type foreligger?
Tamkreft utvikles i mer enn 90% av tilfellene fra overflate-epitelet i slimhinnen som består av kjertler. Kreftsvulsten danner da unormale kjertelformasjoner og kalles adenokarsinom.
Bilde av tarmkreft sett i mikroskopet
Svulstens differensieringsgrad avhenger av hvor mye den avviker fra normalt vev:
- Lavgradig malign (tidligere kalt høyt til middels differensiert), svulsten avviker forholdsvis lite
- Høygradig malign (tidligere kalt lavt differensiert), svulsten avviker mye fra normalvev
Omtrent 20 % av adenokarsinomene er høygradig maligne og prognosen er da dårligere enn for de lavgradig maligne svulstene. Noen svulster produserer mye slim som ligger som sjøer mellom fast svulstvev, og kalles da «mucinøse»». Disse har også dårligere prognose.
Det finnes andre, svært sjeldne typer av karsinomer i tarmen, så som signetring-celle karsinom, plateepitel karsinom, adenoskvamøst karsinom, medullært karsinom og udifferensiert karsinom. Det finnes også andre krefttyper i tarmen, herunder lymfom, nevroendokrin svulst og sarkomer – såkalt Gastrointestinal stromal tumor (GIST).
Utbredelse
Patologen bestemmer svulstens dybdevekst og eventuell innvekst i naboorganer, om det foreligger spredning til lymfeknuter eller til isolerte minisvulster i fettvevet utenfor tarmveggen (kalles "tumor deposits") og om det foreligger tegn til karinnvekst inne i tarmveggen og/eller utenfor tarmveggen.
Reseksjonsmarginer/Residual tumor
Patologen måler minste avstand fra hovedsvulsten, og fra eventuell lymfeknutespredning og fra eventuell karinnvekst og til den kirurgiske reseksjonsflaten (der kirurgen har delt vevet på utsiden av tarmen og det omgivende fettvevet/krøset).
R0:Dersom avstanden er mer enn 1 mm og det ikke ved øvrige undersøkelser er påvist kreftspredning sier man at det er gjort en R0-reseksjon fordi det ikke er tegn til residual (R) tumor (gjenværende svulst).
R1: Dersom avstanden mellom hovedsvulsten, lymfeknute med spredning eller karinnvekst måles til kun 0-1 mm, antar man at det kan være latt tilbake mikroskopisk sykdom og dette klassifiseres som R1-reseksjon.
R2: Dersom man vet at det er tilbake makroskopisk synlige rester av primærtumor eller det er påvist fjernmetastaser som ikke er fjernet, klassifiserer man operasjonen som en R2-reseksjon.
Effekt av forbehandling
Hos pasienter som får forbehandling med bestråling og/eller med cellegift kan man vurdere effekten av behandlingen (responsen) ved røntgenbilder tatt før og etter behandlingen. Effekten kan også vurderes ved mikroskopi av svulsten som er tatt ut, der man vurderer hvor stor andel av svulsten som nå består av kreftceller og hvor stor del av den som består av arrvev. Dette kalles Tumor Regression Grade (TRG), og man bruker enten en 3-delt eller 5-delt skala for klassifisering. God respons på forbehandlingen gir gunstigere prognose.
Bildeeksempel på tumor regresjons-grad (TRG) 1–5 etter forbehandling
Klinisk – patologisk stadium
Basert på funn ved alle forundersøkelser, funn under operasjonen og patologens undersøkelse av operasjonspreparatet får man fasit på hva som er sykdomsstadium ved diagnose og gjennomført primærbehandling. På dette grunnlag kan man da fastsette det endelige klinisk-patologiske stadium. Det vanlige brukte systemet for å klassifisere kreft, inklusive tarmkreft er TNM-systemet (Tumor-Node-Metastases):
T= Tumor (primærtumors dybdevekst)
N= Node (lymfeknuter, status for metastaser)
M= Fjernmetastaser
Bildeserie av ulike stadier
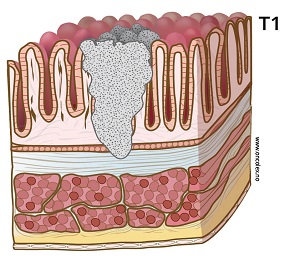
T1: Svulsten vokser inn i submukosa, men ikke dypere.

T1: Kan deles i undergrupper, Kikuchi i klassifisering, sm1-sm2-sm3.
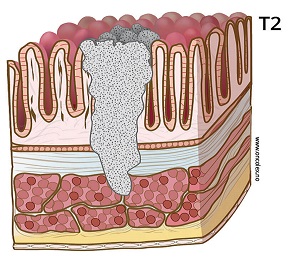
T2: Svulsten vokser ned i muskellaget/ytre del av tarmveggen.
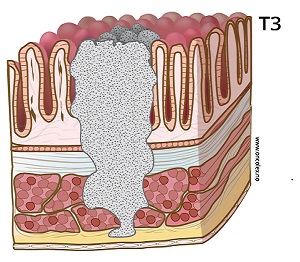
T3: Svulsten vokser gjennom hele tarmveggen og ut i fettvevet omkring tarmen.
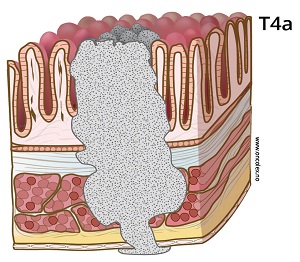
T4a: Svulsten vokser inn i og gjennom bukhinnen som kler tarmveggens utside (serosa).
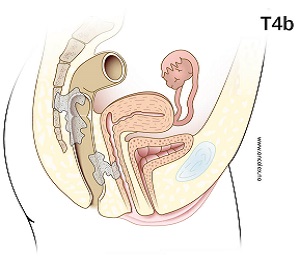
T4b: Svulsten vokser inn i naboorgan, her i vaginas bakvegg.
T-stadium - tumors dybdevekst (se figurer ovenfor)
- Tis Karsinoma in situ ("Tumor in situ" = grov celleforandring i slimhinnen)
- T1 Vokser inn i submukosa, men ikke gjennom denne.
- T1 kan inndeles i undergrupper
- Kikuchi sm1 - svulsten vokser til øverste laget av submukosa
- Kikuchi sm2 - svulsten vokser til midtre lag av submukosa
- Kikuchi sm3 - svlsten vokser til dypeste lag av submukosa
- T2 Innvekst i muskellaget (muscularis propria)
- T3 Innvekst gjennom muskellaget og inn i fettvevet utenfor
- T4a Innvekst/gjennomvekst i bukhinnen/serosa
- T4b Innvekst i naboorgan
N-stadium = Lymfeknutestatus
- N0 Ikke påvist spredning til lymfeknuter
- N1 Spredning til inntil 3 lymfeknuter
- N1a Spredning til 1 lymfeknute
- N1b Spredning til 2–3 lymfeknuter
- N1c Spredning til isolert(e) tumorknute(r) i fettvev (tumor deposits)
- N2 Spredning til 4 eller flere positive lymfeknuter
- N2a Spredning til 4–6 lymfeknuter
- N2b Spredning til > 7 lymfeknuter
M-stadium = Fjernspredning
- M0 Ingen fjernspredning
- M1 Fjernspredning påvist
- M1a Metastase til ett organ (peritoneum ikke affisert)
- M1b Metastase til to eller flere organer (peritoneum ikke affisert)
- M1c Metastase til peritoneum, med eller uten andre metastaser
Det er vanlig med et prefix for å angi hva slags undersøkelse som ligger til grunn for det angitte TNM-stadium:
- cTNM - klinisk stadium før operasjonen ut fra klinisk undersøkelse inkludert endoskopi og CT
- mrTNM - stadium basert på MR-undersøkelse
- pTNM - stadium basert på histo-patologisk undesøkelse (vevsprøve av operasjonspreparat)
- ypTNM - histo-patologisk undersøkelse av operasjonspreparatet hos pasient som har fått strålebehandling før operasjon.
Les mer om T-stadium tumors dybdevekst
Basert på T, N og M-stadium kan man nå skille mellom over 80 ulike stadier, men for praktiske formål velger man vanligvis klassifisering i 4 ulike stadier, basert på prognostisk betydning. Den såkalte UICC/AJCC og Dukes´ tradisjonelle stadieinndelingen ses nedenfor.
UICC/AJCC/TNM stadier /Dukes´stadier, klassifisering i 4 ulike stadier
UICC stadier/Dukes´/TNM
|
UICC
|
DUKES´
|
T
|
N
|
M
|
| I |
A |
T1-T2 |
N0 |
M0 |
| II |
B |
T3-T4 |
N0 |
M0 |
| III |
C |
Alle T
|
N1-N3 |
M0 |
| IV |
D |
Alle T |
Alle N |
M1 |